- Neue Artikel
- Was Patienten sagen – Fortsetzung
- Praxis/ online Terminvergabe
- Warum die Diagnose einer psychosomatischen Erkrankung häufig eine Fehldiagnose ist
- Gefäßkompressionssyndrome
- Haben Sie Fragen?
- Checkliste Gefäßkompressionssyndrome
- Beschreibung Ihrer Symptome
- Erklärung der geschlechtsspezifischen Unterschiede bei den klinischen Symptomen von abdominalen vaskulären Kompressionssyndromen: Varikozele und Penis-/Hodenschmerzen – ihre Hauptmanifestation bei Männern.
- Die Varikozele wird überwiegend durch eine Kompression der linken Nierenvene verursacht
- Muskuloskelettale Besonderheiten der weiblichen Pubertät
- Lordose /Hohlkreuz – Ursache zahlreicher abdomineller Kompressionssyndrome
- Die Anhebung einer Vene erzwingt deren Kompression
- Truncuskompression bei Kindern
- Lordogenetisches Mittellinensyndrom
- Neurologische Folgen des Mittellinienstauungssyndroms
- Erfolgreiche Behandlung einer Teenagerin, die aufgrund extremer postprandialer Schmerzen nicht essen und aufgrund einer Spastik im linken Bein nicht gehen konnte.
- Schwere Ataxie bei einer jungen Frau mit schwerer venöser Rückenmarksstauung – vollständige Heilung nach Dekompression der linken Nierenvene
- Alle abdominalen Kompressionssyndrome liegen in der Lordose begründet
- Das „Nussknacker“-Syndrom ist eine Fehlbezeichnung
- May-Thurner-Konstellation /May-Thurner-Syndrom/Cockett’s syndrome/Vena iliaca-Kompressionssyndrom
- Mittelliniensyndrom (Stauung der Mittellinienorgane)
- Pelvines Kongestionssyndrom
- Truncus-coeliacus-Kompression / Dunbar-Syndrom / MALS / Ligamentum arcuatum-Syndrom
- Wilkie-Syndrom / Arteria-mesenterica-superior-Syndrom
- Kompression der Vena cava inferior
- Quantifizierung der Gefäßkompressionssyndrome mit der PixelFlux-Technik
- Bindegewebserkrankungen begünstigen kombinierte Kompressionssyndrome
- Posturales Tachykardiesyndrom (POTS) – die hämodynamische Folge von Gefäßkompressionssyndromen und lockerem Bindegewebe
- Unruhige Beine (restless legs) – Folge venöser Kompressionssyndrome
- Pudendusneuralgie bei vaskulären Kompressionssyndromen
- Ein neues sonographisches Zeichen für eine schwere orthostatische Beckenvenenstauung
- Migräne und Multiple Sklerose
- Behandlung von Kompressionssyndromen
- Fehler bei der Therapie von Gefäßkompressionssyndromen
- Embolisation – Irrweg bei venösen Kompressionssyndromen
- Risiken von Stents bei venösen Kompressionssyndromen
- Chirurgische Behandlung von abdominalen Kompressionssyndromen: Die Bedeutung der Bindegewebshypermobilität
- Nutcracker and May-Thurner syndrome: Decompression by extra venous tube grafting and significance of hypermobility related disorders
- Chronisches regionales Schmerzsyndrom (CRPS) verursacht durch Venenkompressionen und mechanische Reizung des Plexus coeliacus
- Vaskuläre Kompressionssyndrome, die ich kürzlich entdeckt habe
- Kaleidoskop lehrreicher Krankheitsverläufe
- Eine venöse Stauung im Rückenmark kann möglicherweise zur Entwicklung einer Querschnittslähmung bei Patienten mit spinaler Muskelatrophie beitragen.
- Ultraschalldiagnostik
- Leistungsspektrum
- Funktioneller Farbdoppler-Ultraschall – wie ich ihn verstehe
- Durchblutungsmessung – PixelFlux-Verfahren
- Forschung
- Publikationen
- Nutcracker and May-Thurner syndrome: Decompression by extra venous tube grafting and significance of hypermobility related disorders
- Veröffentlichungen von Th. Scholbach
- Eigene Publikationen
- Erstbeschreibung der Bestimmung des Gewebsperfusionsindexes in Nierentranplantaten
- Erstbeschreibung des Mittellininesyndroms – Aspirintherapie
- Erste sonografische Gewebsperfusionsmessung in Nierentransplantaten
- Erste sonografische Tumorperfusionmessung und Korrelation zur Tumoroxygenierung
- Erstmalige Darmwandperfusionsmessung bei M. Crohn
- Erstmalige sonografische Gewebsperfusionmessung der Nieren
- Erstmaliger Nachweis von Frühveränderungen der Nierenperfusion bei Diabetes mellitus
- PixelFluxmessung der Nierengewebsperfusion
- Publikationen
- Expertise
- Bornavirusinfektion
- Wissenschaftliche Zusammenarbeit
- Cookie-Richtlinie
- Hinweise zu medizinischen Erläuterungen
- Datenschutzerklärung
- Cookie Policy (EU)
- Impressum

Eine venöse Stauung im Rückenmark kann möglicherweise zur Entwicklung einer Querschnittslähmung bei Patienten mit spinaler Muskelatrophie beitragen.
Vorwort
Seit über 35 Jahren bin ich auf die Diagnose und Behandlung von Gefäßkompressionen spezialisiert. In dieser Zeit habe ich viele Patienten mit Beinschwäche behandelt, von denen einige so stark betroffen waren, dass sie nicht mehr gehen konnten und entweder bettlägerig waren oder einen Rollstuhl benötigten. Alle diese Patienten litten unter einer venösen Wirbelsäulenstauung aufgrund einer Gefäßverbindung zwischen der unter Druck stehenden und komprimierten linken Nierenvene und dem Rückenmark.
Dieses Gefäß wurde erstmals von französischen Anatomen identifiziert und daher auf Französisch „tronc réno-rachidien” genannt. Dies bedeutet auf Deutsch „Nieren-Wirbelsäulen-Stammgefäß“. Nach erfolgreicher Dekompression der linken Nierenvene und der linken Beckenhauptvene, die bei Patienten mit Kompression der linken Nierenvene häufig gleichzeitig komprimiert ist, gewannen diese Patienten ihre Muskelkraft in den Beinen zurück und konnten wieder gehen.
Aus diesem Grund sah ich Ähnlichkeiten zwischen diesen Patienten und denen mit spinaler Muskelatrophie SMA II, II und IV, bei denen die Beinmuskulatur früher und stärker betroffen ist als die Muskeln des Oberkörpers.
Obwohl alle diese Erkrankungen durch einen Defekt im SMN-1-Gen verursacht werden, fragte ich mich, warum sie in den Beinen beginnen und erst später die Arme und den Oberkörper betreffen.
Die schwersten Formen mit sehr frühem Ausbruch, SMA 0 und SMA I, folgen diesem Muster jedoch nicht: Bei SMA 0-Patienten besteht schon bei der Geburt eine Gesichtslähmung, während bei SMA I die Gesichtsmuskeln zunächst verschont bleiben, später jedoch ebenfalls betroffen sind und die Muskeln des gesamten Körpers von Anfang an betroffen sind.
Da ich viele Patienten mit vaskulären Kompressionssyndromen und spinaler Stauung behandelt habe, die zu einer Schwäche der Beine führen, habe ich mich gefragt, ob eine spinale Stauung zur Schweregrad und zum Fortschreiten der spinalen Muskelatrophie beitragen könnte.
Eine Blutstauung tritt auf, wenn venöses Blut aufgrund einer Kombination aus anhaltendem arteriellen Zufluss und behindertem venösen Abfluss Druck auf ein Organ ausübt oder wenn zusätzliches venöses Blut in ein Gefäßgebiet gelangt, sobald das Organ Teil eines Umgehungskresilaufes von eingeengten Venen wird.
Innerhalb des zentralen Nervensystems können wir formal zwischen einer Stauung des Gehirns und einer Stauung der Wirbelsäule unterscheiden. Eine Stauung des Gehirns betrifft in erster Linie das Gehirn selbst und die Hirnnerven, die die Muskeln von Gesicht, Hals und Schultern innervieren. Aufgrund der umfangreichen Verbindung zwischen Rückenmark und Schädel am Foramen magnum an der Schädelbasis kann sich der Druck innerhalb dieser Strukturen je nach Körperhaltung verschieben.
Eine Stauung der Wirbelsäule würde die Spinalnerven beeinträchtigen, abhängig vom hydrostatischen Druck der stauenden Flüssigkeit – in diesem Fall venöses Blut. Bei aufrechter Wirbelsäule ist der Druck im Lenden- und unteren Brustbereich höher als im oberen Brust- und Halsbereich. Bei horizontaler Wirbelsäule verteilt sich der Druck jedoch gleichmäßig über die gesamte Wirbelsäule.
Aus Sicht der Stauung des Zentralnervensystems würde es zu einer Schädigung der Muskeln von Kopf, Nacken und Schultern kommen, wenn das Gehirn gestaut ist. Genau das ist bei SMA Typ 0 zu beobachten, der bereits beim Feten beginnt. Im Gegensatz zu SMA Typ I, der in den ersten Lebensmonaten beginnt und die Gesichtsmuskeln verschont, betrifft SMA Typ 0 von Anfang an die Gesichtsmuskeln und auch alle anderen Muskeln.
Bei SMA I könnten die Hirnnerven weniger von einer Stauung des ZNS betroffen als bei SMA 0. Unter der Annahme der hier vorgestellten Theorie liegt das Baby entweder die meiste Zeit horizontal (während es schläft) oder wird von den Eltern mit erhobenem Kopf und gesenkten Beinen gehalten. Dies könnte erklären, warum die Hirnnerven und damit die Gesichtsmuskeln bei Babys mit SMA I in erster Linie nicht betroffen sind und warum die Auswirkungen auf die Arme bei SMA I stärker sind und früher auftreten als bei den Typen II bis IV.
Da der Fötus in der Regel mit dem Kopf nach unten liegt, wenn die Mutter aufrecht sitzt oder steht, wirkt sich die Stauung des ZNS stärker auf den Oberkörper, einschließlich der Hirnnerven, aus als bei SMA-Typen, die später im Leben auftreten, wenn die Patienten bereits den größten Teil des Tages aufrecht sind.
Dies ist bei den SMA-Typen II bis IV der Fall. Sie beginnen im Kindes- oder Erwachsenenalter. Dann wirkt sich die Stauung im ZNS aufgrund des hohen hydrostatischen Drucks in der Lendenwirbelsäule und der unteren Brustwirbelsäule in aufrechter Haltung bei einer Stauung der Wirbelsäule stärker auf die kaudalen Teile des Rückenmarks als auf die kranialen Teile und das Gehirn aus.
Wenn Stauungen eine Rolle bei der Entwicklung einer fortschreitenden Muskelparalyse bei SMA-Patienten spielen, würden die verschiedenen Muster der Muskelschädigung von SMA 0 bis SMA IV zu der Vorstellung passen, dass der höchste Staudruck in dem Teil des ZNS herrscht, der näher an der Erdoberfläche liegt. Die Schwerkraft wirkt in einer vertikalen Linie, sodass der Druck in einer Flüssigkeitssäule unten am höchsten und oben am niedrigsten ist. Unter der Annahme, dass ein höherer Staudruck zu größeren neuronalen Schäden führt, stützt die Tatsache, dass Embryonen und Neugeborene im Oberkörper stärker betroffen sind, während SMA-Patienten mit späterem Ausbruch stärkere Muskelschäden aufweisen, die vom unteren (kaudalen) Teil der Wirbelsäule innerviert werden, diese hydrostatische Theorie eines zusätzlichen Faktors, der den Verlauf der SMA beeinflusst.
95 % der vier Arten von spinaler Muskelatrophie werden durch einen Mangel an SMN (Survival Motor Neuron Protein) verursacht, das vom SMN-1- oder SMN-2-Gen kodiert wird.
Diese vier Arten von SMA unterscheiden sich hinsichtlich des Alters, in dem die klinischen Symptome auftreten, sowie hinsichtlich des Schweregrads ihres Verlaufs und ihrer Prognose.
SMA 0 beginnt schon beim Feten im Mutterleib. SMA I beginnt bei Neugeborenen und Säuglingen und verläuft oft tödlich in der frühen Kindheit. Die unteren Gliedmaßen sind in der Regel schwächer als die oberen Gliedmaßen.
SMA II beginnt im Alter von etwa 6 bis 8 Monaten und betrifft in erster Linie die Beine. Die Kinder erreichen die Fähigkeit zu sitzen nur mit Hilfe.
Patienten mit SMA III lernen, mehr als 10 Schritte zu gehen, und behalten diese Fähigkeit bis ins Erwachsenenalter, wenn auch in den Beinen eine Schwäche einsetzt.
SMA IV ist eine milde Erkrankung mit geringen funktionellen Auswirkungen, wahrscheinlich aufgrund einer erhöhten Anzahl von SMN-2-Kopien.
Interessanterweise beginnen 5 % der SMA-Subtypen, die nicht durch einen SMN-1-Mangel verursacht werden, nicht selten ebenfalls in den unteren Extremitäten.
Fallbericht
Hier berichte ich über eine 64-jährige Patientin mit vier Kopien von SMN2 und fortschreitender Schwäche der unteren Extremitäten, die ab dem Alter von 48 Jahren zeitweise und mittlerweile fast ständig auf einen Rollstuhl angewiesen war.
Anamnese
Die Patientin konnte nur mit Unterstützung aus einer sitzenden Position aufstehen; ein Assistent musste ihren Gürtel hinten hochziehen, während sie ihren Oberkörper mit den Armen auf einen Tisch vor ihr stützte. Sobald sie ihre Knie strecken konnte, legte sie ihre Hände auf den Tisch vor ihr. Aus dieser Vierfüßlerposition konnte sie dann aufstehen, indem sie plötzlich ihre Rumpfmuskulatur anspannte, wodurch die Wirbelsäule wie durch einen Peitschenhieb in eine aufrechte Haltung gebracht wurde.
Abgesehen von ihrer Beinlähmung hatte die Patientin keine weiteren Beschwerden. Sie berichtete weder über Kopfschmerzen noch über Rückenschmerzen. Sie zeigte Anzeichen von hypermobilen Gelenken und lockerem Bindegewebe: Sowohl ihre Ellenbogen- als auch ihre Kniegelenke können überstreckt werden, und früher konnte sie im Stehen mit den Handflächen den Boden berühren. Dies ergibt einen Beighton-Score von 5/9, was auf ein Hypermobilitätssyndrom hindeutet. In jüngeren Jahren konnte sie ihre Beine hinter den Nacken legen. Die Patientin hat keine Striae distensae oder erweiterte subkutane Gefäße am Bauch. Aufgrund chronischer Ödeme in beiden Beinen trägt sie Kompressionsstrümpfe. Bislang wurde dies auf die Immobilisierung der Patientin zurückgeführt.
Klinische Untersuchung
Die Palpation des Abdomens ergibt keine lokalisierten Druckschmerzen oder pathologischen Widerstände. Die Auskultation ist ebenfalls unauffällig, ohne Gefäßgeräusche und mit normaler Peristaltik. Der Bauch ist aufgrund einer extremen Lordose, die aus einer zunehmenden Schwäche der Gesäßmuskulatur resultiert, vorgewölbt. Die Patientin berichtet jedoch, dass sie bereits vor dem Einsetzen der signifikanten Lähmung ihrer Beine eine verstärkte Lordose hatte.
Quantitative Farbdoppler-Sonographie
Es wird eine Farbdoppler-Sonographie mit Quantifizierung der Gewebedurchblutung der Gebärmutter und der Nieren sowie Durchflussvolumenmessungen in beiden inneren Beckenvenen durchgeführt.
Die Gebärmutter ist massiv vergrößert und weist eine erhebliche Zunahme der venösen Blutgefäße auf, was auf eine schwere Beckenstauung hindeutet, die von der Patientin bisher nicht wahrgenommen wurde.
Die maximale Gewebedurchblutung der Beckenorgane, gemessen unter standardisierten Bedingungen (cm/s * cm² der durchbluteten Fläche des ROI /cm² des ROI – normal < 0,05), beträgt:
Organ Mittelwert (%) Maximalwert (%)
====================================
Uterus 678,0 % 1532,0 % des Normalwertes
Die Quantifizierung der Gewebedurchblutung der Gebärmutter mit der PixelFlux-Technik zeigt eine massive Stauung der Gebärmutter.
Die Messung des Durchflussvolumens in beiden inneren Beckenvenen zeigt eine auffällige Asymmetrie der Beckenvenendrainage. Die linke innere Beckenvene transportiert 96 ml/min nach kranial und das Gefäß ist schlank, während die rechte viel breiter ist und 960 ml/min nach kranial transportiert. Anstelle einer gleichmäßigen Drainage mit einem Transportvolumen von 50 % auf jeder Seite transportiert die linke Seite nur 9 %, während die rechte Seite über 91 % übernimmt.
Die Ursache für die starke Beckenstauung ist die erhebliche Kompression der linken Beckenhaiptvene am oberen Ende ihres Verlaufs über dem Promontorium. Diese Kompression tritt nicht direkt am May-Thurner-Punkt auf, wo die Vene die rechte Beckenarterie kreuzt. Während die Vene links vom Kreuzbein eine sagittale Breite von 11 mm aufweist, wo der Blutfluss unterhalb der Erkennungsschwelle liegt, führt die trichterförmige Verengung der Vene beim Aufstieg zum Promontorium zu einem intermittierenden Blutfluss im komprimierten Abschnitt unmittelbar ventral zum vierten Lendenwirbelkörper entlang der Mittellinie. Hier hat die Vene eine sagittale Breite von weniger als 1 mm, was zu einer Blutflussgeschwindigkeit von bis zu 132 cm/s führt. Der Blutfluss kann jedoch nur während der Inspiration nachgewiesen werden. Es handelt sich also um einen schweren Fall von Beckenvenenstauung (pelviner Kongestion) durch eine Spielart des May-Thurner-Syndroms, wobei Beinödeme die einzige klinische Manifestation sind.
Eine detaillierte Untersuchung zeigt eine links aufsteigende Lendenvene mit kranial gerichtetem Blutfluss, die ein Volumen von etwa 72 ml/min transportiert, was wahrscheinlich zur spinalen Stauung beiträgt.
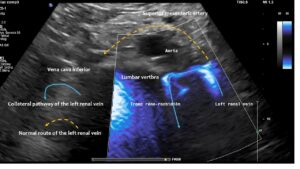
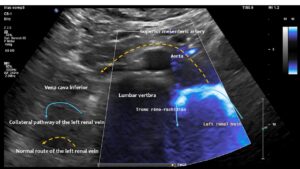
Anstatt sich zwischen der Aorta und oberer Damrarterie von links nach rechts zur Vena cava zu ziehen, verläuft die linke Nierenvene um den linken seitlichen Umfang der Wirbelsäule und leitet das Blut über ein starkes Gefäß, einen Tronc réno-rachidièn , zur Wirbelsäule und in den Spinalkanal ab. Zusätzlich ist eine sehr schmale retroaortale zweite linke Nierenvene vorhanden.
Diese Bilder, die von vorne aufgenommen wurden, zeigen den Tronc réno-rachidièn. Dieses Gefäß verläuft in einer U-Kurve entlang der linken Seite der Lendenwirbelsäule nach hinten, tritt in das Foramen intervertebrale ein und übt so Druck auf den Wirbelkanal aus. Sie zeigen, dass der präaortale Teil der linken Nierenvene (gelber gestrichelter Pfeil) kein Blut transportiert, was bedeutet, dass das gesamte linke Nierenvenenblut über den Tronc réno-rachidièn umgeleitet werden muss. Der andere natürliche Kollateralweg, die linke Eierstockvene, ist hier weniger bedeutend. Bei dieser Patientin (wie bei vielen Arterien mit Kompression der linken Nierenvene) wird die Kollateralisation über die linke Eierstockvene zum Beckenvenenkreislauf durch die Kompression der linken Beckenhauptvene behindert. Diese Kombination ist sehr häufig und erfordert die gleichzeitige Behandlung der linken Nierenvene und der linken Beckenhauptvene in einer Operation, indem beide mit einer PTFE-Abdeckung abgeschirmt werden.
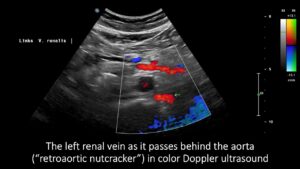
Das Blut im Tronc réno-rachidièn wird pulsierend moduliert, was eine rhythmische Kompression der linken Nierenvene zwischen der Aorta und der A. mesenterica superior beweist. Diese Kompression ist so ausgeprägt, dass ventral zur Aorta kein Blutfluss sichtbar ist, sondern die Druckwelle zum Kollateralgefäß dem Tronc réno-rachidièn übertragen wird.
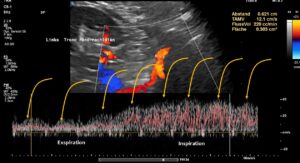 Dieses Bild zeigt die Übertragung des pulsierenden Drucks der Aorta und der A. mesenterica superior auf den Tronc réno-rachidièn (gelbe Pfeile). Beide Arterien drücken den letzten Abschnitt der linken Nierenvene vollständig zusammen und behindern so den gesamten Blutfluss, aber der Druck wird rhythmisch auf den Wirbelkanal und damit auf das Rückenmark übertragen. Nicht selten entwickeln betroffene Patienten Kopfschmerzen und Migräne, was bei diesem Patienten jedoch nicht der Fall war.
Dieses Bild zeigt die Übertragung des pulsierenden Drucks der Aorta und der A. mesenterica superior auf den Tronc réno-rachidièn (gelbe Pfeile). Beide Arterien drücken den letzten Abschnitt der linken Nierenvene vollständig zusammen und behindern so den gesamten Blutfluss, aber der Druck wird rhythmisch auf den Wirbelkanal und damit auf das Rückenmark übertragen. Nicht selten entwickeln betroffene Patienten Kopfschmerzen und Migräne, was bei diesem Patienten jedoch nicht der Fall war.
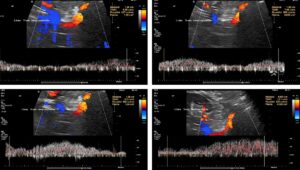 Diese Bilder zeigen die Atemvariabilität des Volumentransportes im Tronc réno-rachidèn.
Diese Bilder zeigen die Atemvariabilität des Volumentransportes im Tronc réno-rachidèn.
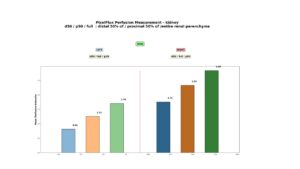
Das folgende Diagramm zeiget die PixelFlux-Messung des Blutflusses im Nierenparenchym. Es besteht eine signifikante Verringerung des Blutflusses zur linken Niere. Dies ist auf eine schwere venöse Abflussbehinderung durch die vollständig komprimierte linken Nierenvenen sowohl prä- als auch subtotal in retroaortaler Position zurückzuführen. Die linke Niere erhält nur 53 % des Perfusionsvolumens der rechten Niere. Die periphere Parenchymperfusion ist auf der linken Seite ebenfalls deutlich geringer als auf der rechten Seite, was den Stauungsdruck im Wirbelkanal widerspiegelt. Dies verhindert, dass der Tronc réno-rachidien mehr Blut aus der linken Nierenvene ableitet und so die Niere entlastet. Umgekehrt zeigt dies den erheblichen Druck, der auf den Wirbelkanal und damit auf das Rückenmark ausgeübt wird, der somit ein wesentlicher Faktor für die Paraparese der Patientin sein kann.
Diagramm der Perfusionsmessung des Nierenparenchyms mit der PixelFlux-Technik
Die Säulen zeigen die Perfusionsintensität in cm/s, berechnet als Perfusionsgeschwindigkeit [cm/s] aller farbigen Pixel multipliziert mit der Fläche aller farbigen Pixel [cm²] geteilt durch die Fläche aller Pixel im gesamten interessierenden Bereich [cm²].
 Die folgenden Videos der MR-Venografie der Patientin bestätigen und veranschaulichen die sonografischen Befunde. Allerdings ist der Ultraschall aussagekräftiger als das MRT, da er die Flussrichtung und die Flussvolumina in den Kollateralgefäßen messen und die Nierenperfusion beider Seiten vergleichen kann. Daraus lässt sich der Druck im Spinalkanal ableiten, der die Lähmung der Beine verstärken und beschleunigen kann.
Die folgenden Videos der MR-Venografie der Patientin bestätigen und veranschaulichen die sonografischen Befunde. Allerdings ist der Ultraschall aussagekräftiger als das MRT, da er die Flussrichtung und die Flussvolumina in den Kollateralgefäßen messen und die Nierenperfusion beider Seiten vergleichen kann. Daraus lässt sich der Druck im Spinalkanal ableiten, der die Lähmung der Beine verstärken und beschleunigen kann.
Auch bei einer zweiten Patientin mit spinaler Muskelatrophie wurden erhebliche venöse Gefäßkompressionen mit unzureichenden Kollateralkreisläufen sowie Hinweise auf eine Stauung des Rückenmarks festgestellt. Die folgende Videozusammenfassung beschreibt die sonografischen Befunde und erklärt den pathophysiologischen Effekt unzureichender Kollateralkreisläufe, der mithilfe der PixelFlux-Messung der renalen Parenchymperfusion aufgedeckt werden kann.
Diskussion
Dies ist die erste Beschreibung einer spinalen Stauung bei einem Patienten mit fortschreitender Lähmung beider Beine, die bislang ausschließlich einer spinalen Muskelatrophie Typ III (SMA III) zugeschrieben wurde. Es ist jedoch bekannt, dass auch Patienten ohne genetischen Defekt des SMN-1-Gens eine Paraparese entwickeln können. Dies wurde 1977 in einer Veröffentlichung von Frantz, Aboulker, Küss und Jardin beschrieben. Sie beschreiben die Entwicklung einer Paraplegie bei Patienten mit einer Obstruktion der linken Nierenvene und der Entwicklung eines Tronc réno-rachidièn und einer anschließenden Stauung des Rückenmarks. Diese Autoren behandelten die Paraplegie erfolgreich durch Ligatur des Tronc réno-rachidièn.Dies führte jedoch bei einem ihrer beiden Patienten zu einer Nierenschädigung. In einer später veröffentlichten Arbeit konnten sie deutlich bessere Ergebnisse erzielen. Allerdings haben sie die Kompression der linken Nierenvene nie beseitigt, was bei der Unterbindung des Tronc réno-rachidièn zu höheren Risiken führt, sofern keine weiteren suffizienten Kollateralen bestehen. Der Zusammenhang zur Kompression der linken Nierenven war französichen Autoren dennoch wohlbekannt.Highlighted Les afferences veineuses reno-rachidiennes dans les myelopathies - Aboulker, Jardin - Unknown copy
Eine andere französische Arbeitsgruppe geht der venösen Stauung bei Myelopathie in nach und bestätigt unsere Beobachtung, dass häufig zahlreiche venöse Gefäßkompressionen gleichzeitig vorkommen und zur Stauung des Rückenmarks mit entsprechenden klinische Folgen beitragen. Diese extrem aufschlussreiche Arbeit stelle ich daher hier zur Verfügung.
Highlighted aubin-et-al-1975-phlébographie-cavo-rachidienne-dans-les-myelopathies-d-origine-veineuse copyUnser Vorgehen ( Sandmann/Schobach) beseitigt die Ursache der Rückenmarksstauung durch Dekompression der linken Nierenvene mit deren Umhüllung mit einer PTFE-Hülse. Der Tronc réno-rachidièn versiegt dann automatisch.
Wir (Thomas Scholbach) stellten die Diagnose und (Wilhelm Sandmann) behandelten mehrere Patienten mit einem Tronc réno-rachidien aufgrund einer schweren Kompression der linken Nierenvene und einer daraus resultierenden progressiven Querschnittslähmung, die den Einsatz eines Rollstuhls erforderlich machte. Dadurch konnten die von Frantz et al. 1977 beschriebenen Nierenschäden vermieden und die Gehfähigkeit der Patienten wiederhergestellt werden. Nach der Dekompression der komprimierten Venen konnten sie wieder gehen und anderen normalen täglichen Aktivitäten nachgehen, darunter Tanzen und Surfen.
Die französische Gruppe war in 21 Fällen von Myelopathien und 9 Fällen von Syringomyelie bei der Ligatur des Tronc rèno-rachidièn erfolgreich..iHighlighted Responsabilité de la Veine Rénale Gauche et de la Veine Cave Inférieure Dans Certains cas de Myélites et de Syringomyélie Intéret de la Ligature du Tronc Veineux Réno-Rachidien
Es ist daher denkbar, dass bei Patienten mit einem genetischen Defekt, der zu Muskelschwäche führt, eine zusätzliche Stauung des Rückenmarks zur Querschnittslähmung beitragen kann, zumal die Schwäche der Gesäßmuskulatur eine Hyperlordose begünstigt. Diese ist der Hauptgrund der venösen Kompressionssyndrome bei Erwachsenen und Adoleszenten.
Aus hämodynamischer und gravitationsmedizinischer Sicht ist es verständlich, dass eine Stauung im Rückenmark aufgrund der aufrechten Körperhaltung des Menschen während des Tages bei SMA II–IV in erster Linie die kaudalen Bereiche betrifft. Dies erhöht den Druck in den kaudalen Teilen des Wirbelkanals und beeinträchtigt dadurch das kaudale Rückenmark. Der genaue molekulare Mechanismus dieser Schädigung muss noch weiter erforscht werden, aber die sofortige klinische Wirkung der Dekompression des Rückenmarks durch Verringerung des zusätzlichen venösen Zuflusses aus den Kollateralen der komprimierten Bauch- und Beckenvenen beweist eindeutig den kausalen Zusammenhang zwischen dem Verlust der Muskelfunktion und der Rückenmarksstauung bei Nicht-SMA-Querschnittsgelähmten.
Daher ist es ratsam, bei Patienten mit einer genetischen Diagnose von spinaler Muskelatrophie eine zusätzliche hämodynamische Ursache für die Querschnittslähmung in Betracht zu ziehen. Dies könnte dazu beitragen, das Fortschreiten der Erkrankung zu verlangsamen, indem die Wirbelsäulenstauung durch eine Operation zur Dekompression der linken Nierenvene und der linken gemeinsamen Beckenvene gelindert wird.